科研进展
我所薛婧团队揭示LY6D为胃样细胞亚群的关键干性标志物及其驱动胰腺肿瘤演进的核心作用机制
日期:2026-02-28
2026年1月16日,上海交通大学医学院附属仁济医院—上海市肿瘤研究所薛婧团队在消化道疾病国际权威期刊GUT在线发表题为“LY6D identifies persistent stem-like cells driving pancreatic tumourigenesis”的突破性研究成果。该研究首次发现胃样细胞状态的特异性标志物—LY6D,并系统揭示其调控胰腺肿瘤发生发展的核心机制,明确了LY6D⁺胃样细胞在PDAC早期异质性建立及肿瘤进展中的关键作用,证实LY6D具备作为泛肿瘤阶段预后生物标志物和治疗靶点的双重价值,为PDAC的临床诊治提供了新思路。
胰腺导管腺癌(Pancreatic ductal adenocarcinoma,PDAC)作为恶性程度极高的肿瘤,早期诊断困难与细胞异质性介导的治疗抵抗是一直是临床诊疗的核心瓶颈。已知致癌性KRAS突变与胰腺炎症损伤的协同作用,可驱动腺泡—导管化生(ADM)并向胰腺上皮内瘤变(PanIN)演进,最终发展为侵袭性PDAC;近些年随着单细胞技术的发展,增加了这一病理演进过程的复杂性。研究鉴定出癌前病变阶段存在多个细胞亚群/状态(如胃样细胞、簇状样细胞、神经内分泌样细胞等),在肿瘤早期发生阶段进一步加大胰腺癌的异质性,有可能成为未来治疗抵抗的重要根源。因此,解析早期病变异质性的调控机制、挖掘关键驱动分子与标志物,成为突破 PDAC 诊疗瓶颈的重要研究方向。
研究团队通过对比胰腺炎及胰腺炎诱导肿瘤模型的单细胞转录组数据,成功捕获到一群具有持续干细胞样特性的LY6D⁺胃样细胞亚群。该亚群起源于携带KRAS突变的ADM病变,具备保守的转录组特征与增强的氧化磷酸化代谢水平,这一代谢优势使其能够长期存活并维持高致瘤潜能。功能学验证进一步证实,LY6D并非单纯的干细胞样细胞标志物,更是维持胃样细胞谱系特性和促进肿瘤进展的关键驱动因子:在KRAS突变背景下,敲除Ly6d可显著延缓炎症驱动的肿瘤进展;而过表达Ly6d则会显著增强肿瘤的致瘤性与转移潜能。深入的机制研究发现,LY6D 通过募集细胞膜脂筏相关激酶互作网络,激活FOSL1介导的表观遗传-转录重编程过程,进而调控肿瘤的发生发展。
在临床转化层面,通过多个公开的人PDAC单细胞转录组测序数据集的分析,发现LY6D阳性胰腺癌细胞亚群表现出高干细胞特性及增强的上皮-间质转化特征,且与患者不良预后密切相关。进一步的临床样本分析显示,LY6D高表达是PDAC患者预后不良的独立危险因素。此外,由于GPI蛋白可被剪切进入血液,对PDAC患者血浆样本的检测分析表明,可溶性LY6D同样具备评估预后的临床价值。
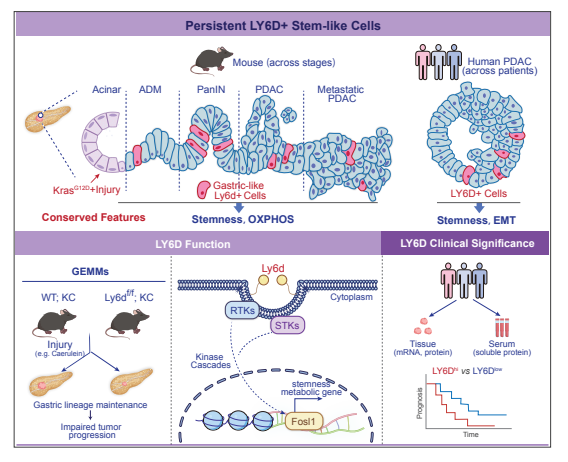
该研究首次证实LY6D⁺胃样细胞状态是介导PDAC早期细胞异质性与肿瘤进展关联的关键驱动因素,不仅填补了胃样细胞亚群调控机制领域的研究空白,更确立了LY6D作为 PDAC 特异性生物标志物的临床价值。这一发现为 PDAC 的早期诊断、预后评估及靶向治疗策略开发提供了全新思路。
上海市肿瘤研究所薛婧研究员为本文通讯作者,住院医师石娟娟、博士生王显、唐莹莹、孟世昕、张争艳为论文的共同第一作者。
原文链接:https://gut.bmj.com/content/early/2026/01/16/gutjnl-2025-336460
