科研进展
我所金浩杰研究员和Rene Bernards院士合作在Nature Reviews Drug Discovery杂志发表长篇综述文章:癌症联合靶向治疗的背景、优势与挑战
日期:2023-01-13近日,我所金浩杰研究员与René Bernards院士作为共同通讯作者在Nature Reviews Drug Discovery期刊上发表了长篇综述文章“Rational combinations of targeted cancer therapies: background, advances and challenges”,对癌症联合靶向治疗策略的背景、优势及面临的挑战进行全面梳理和总结[1]。

20世纪40年代首次使用化疗药物治疗癌症的临床结果表明,单一化疗药物治疗只能暂时缓解癌症进展,且易使肿瘤产生耐药性,由此促成了使用联合化疗来克服耐药性的研究[2]。自20世纪80年代起,对癌症生物学特性和致癌基因的认知极大地促进了癌症靶向治疗的发展。然而,人们很快发现,同化疗类似,癌症的单药靶向治疗依然无法避免耐药的问题,因此寻找靶向治疗的联合策略以获得更持久的疗效成为生物医学研究领域的热点。治疗艾滋病的鸡尾酒疗法便是药物联合治疗的成功案例,说明了药物的联合使用能够实现对疾病的长期控制。因此,该综述重点讨论了癌症靶向治疗产生耐药的机制,以及如何量身定制联合治疗策略来克服这些不同机制的耐药性,并探讨了临床开发这些药物联合治疗的研究策略、挑战和未来前景。
肿瘤耐药性广义上可分为原发性耐药和获得性耐药。前者在使用抗肿瘤药物前就存在于肿瘤中,而后者是药物诱导产生,即肿瘤细胞在药物使用前对该药物敏感,而在药物使用后产生耐药。基于对治疗耐药相关的潜在分子机制的深刻理解,合理的药物联合在癌症治疗中具有巨大的应用潜力。
该综述系统地梳理了不同的药物联合方式治疗癌症的原理,例如基因特异性合成致死、药物特异性合成致死、附加杀伤力、致癌信号的双重阻断、多节点抑制、间歇给药、交替给药等(图1)。针对不同肿瘤耐药机制,选择性使用不同的药物组合策略进行联合靶向治疗更有可能实现对疾病的长期控制。
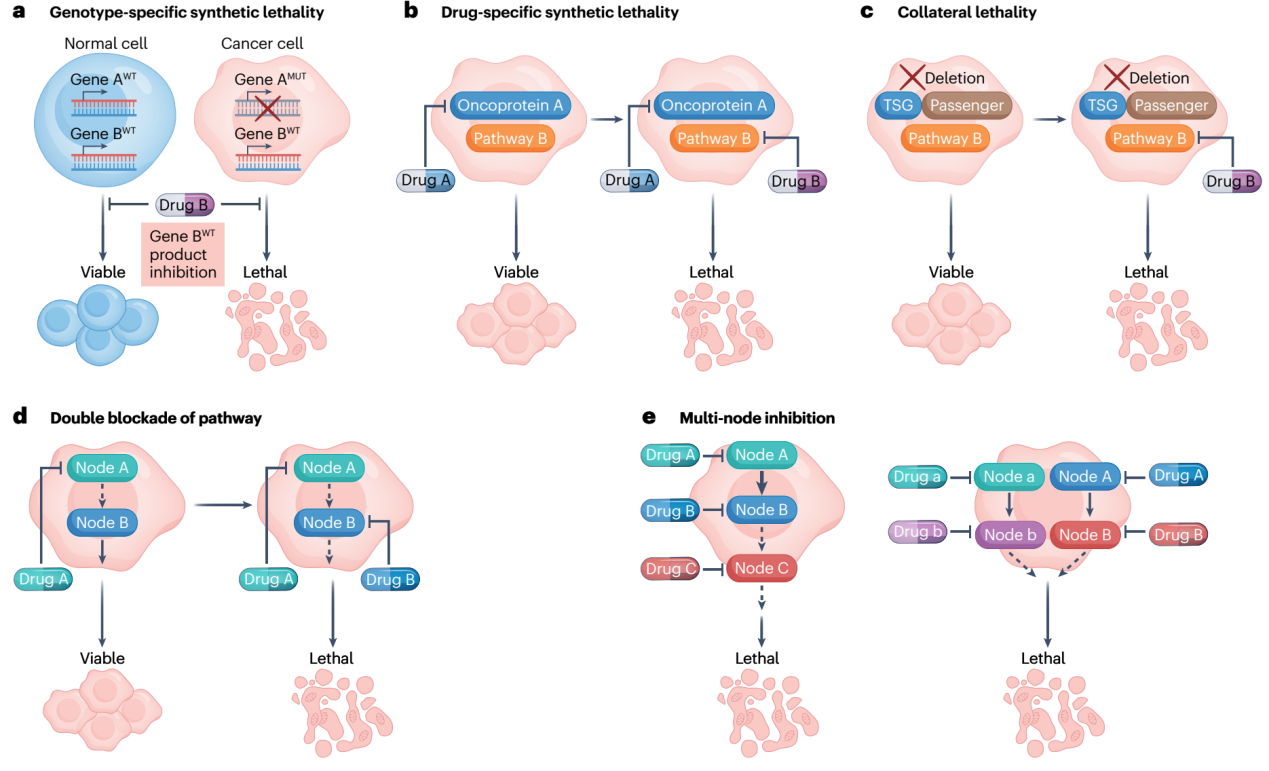
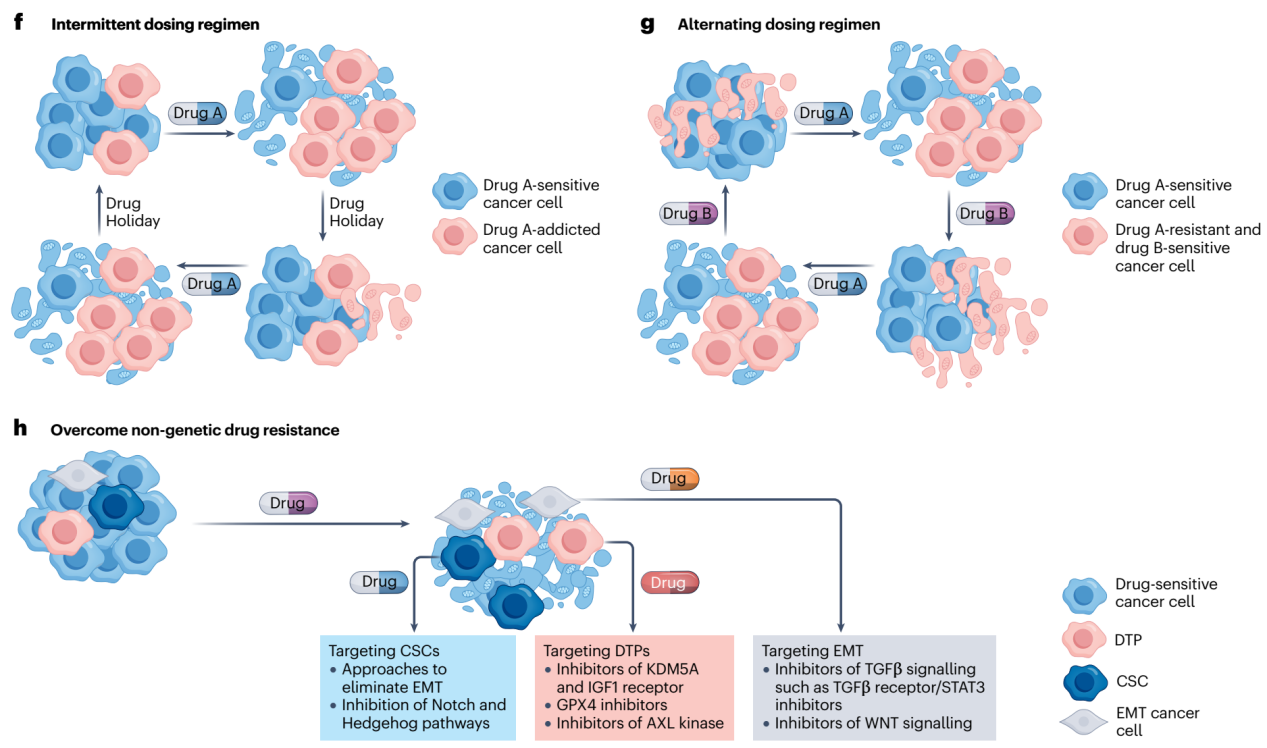
图1 合理的药物组合策略
另外,还有多种基于免疫治疗方法的联合策略,例如cGAS-STING信号通路的激活促进I型干扰素的产生和MHC I类抗原递呈机制的上调,从而增强T细胞对肿瘤细胞的免疫杀伤,因此可以解释人们所观察到的DNA损伤疗法和免疫疗法之间的协同作用;除此之外还有调控T细胞抗肿瘤活性的免疫调节方法等。由此,该综述也总结了目前领域内已被FDA批准的免疫联合疗法(图2)。
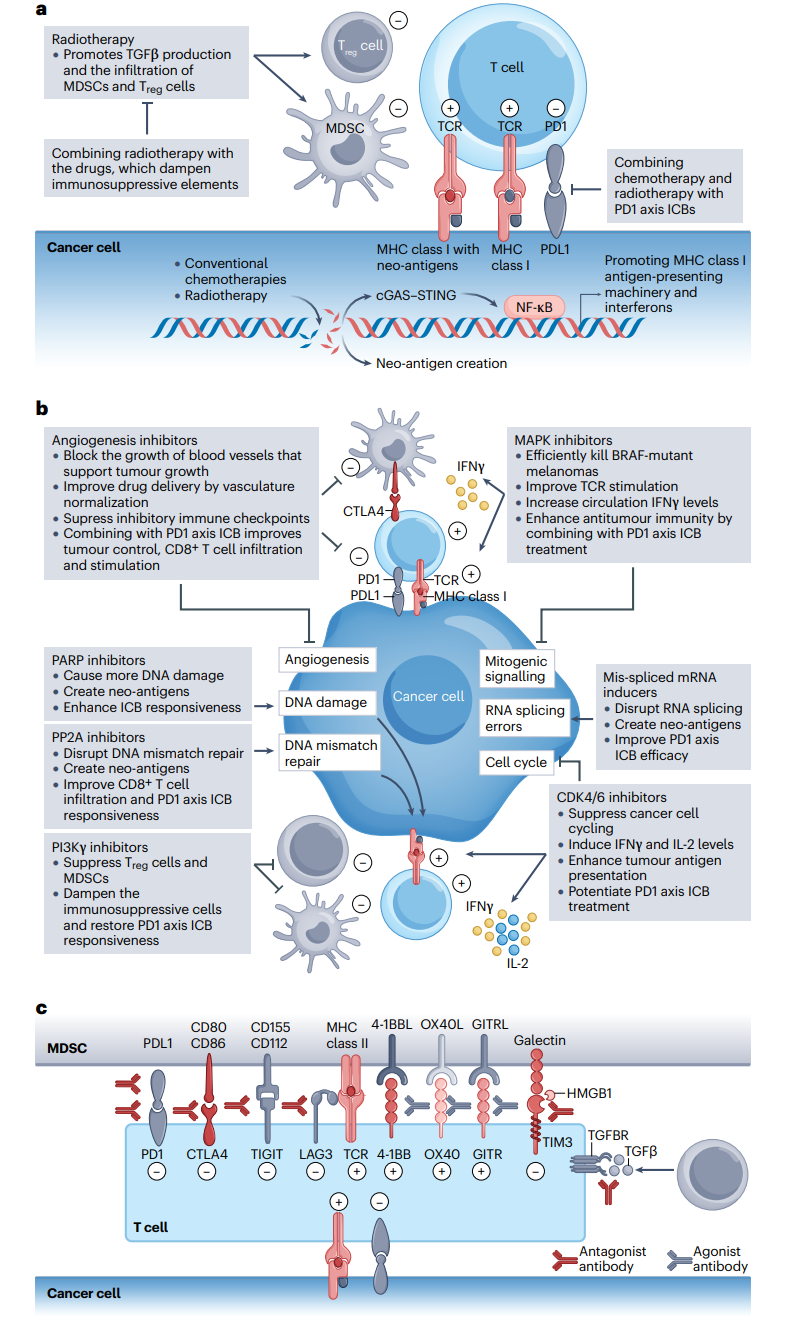
图2 基于免疫疗法的联合策略
最后,该综述还讨论了用于识别有效药物联合的技术,并展望了合理设计联合治疗策略未来在临床上的应用前景和挑战。例如,基于协同致死的概念,在体内外模型中利用以CRISPR-CAS9为基础的高通量功能缺失基因筛选技术(loss-of-function genetic screen)来发现合理高效的药物联合[3]。利用FDA批准上市药物及处于临床研究的化合物进行药物文库的高通量筛选也是发现新的有效药物联合的重要途径之一。而如何整合这些创新性的理念并开展快速高效的开创性临床试验来检验有效的药物组合也需要格外重视。作者还特别强调,如果想在短期内为患者带来更大的临床获益,更好的方法可能来自于现有药物的更优组合而非寻找更多的药物新靶点。
上海市肿瘤研究所金浩杰研究员、中山大学肿瘤防治中心王力勤研究员和荷兰癌症研究所René Bernards院士(美国科学院院士、美国人文与科学院院士、上海交通大学顾问教授)为本文的共同通讯作者。上海交通大学医学院附属仁济医院-上海市肿瘤研究所为第一通讯单位。
参考文献:
[1] Jin H, Wang L & Bernards R. Rational combinations of targeted cancer therapies: background, advances and challenges. Nat Rev Drug Discov. (2022).
[2] Frei, E. III et al. A comparative study of two regimens of combination chemotherapy in acute leukemia. Blood 13, 1126–1148 (1958).
[3] Jin H, et al. EGFR activation limits the response of liver cancer to lenvatinib. Nature. 595, 730-734 (2021).
